«Повелитель времени» (11 класс)
(для решения требуется авторизация)
«Doctor Who? Doctor Who? Doctor Who?» «Доктор Кто», телесериал BBC.
Источник: Всесибирская олимпиада школьников по химии
«Доктор Кто» – самый продолжительный научно-фантастический сериал в мире. Сериал взял свое начало практически 60 лет назад, в 1963 году, а его новые серии выпускаются и по сей день. Доктор – эксцентричный повелитель времени, который сражается с несправедливостью, путешествуя на своей старой машине времени под названием ТАРДИС, часто в сопровождении спутников.
Сегодняшнее путешествие приведет Доктора в гости ко многим знаменитым ученым – основоположникам химической кинетики и катализа, а его спутником выступите Вы, дорогой участник Всесибирской олимпиады.
Первое совместное путешествие привело Вас в 1850 год в гости к Людвигу Вильгельми, который только что опубликовал свою работу «Закон действия кислот на тростниковый сахар», где показал, что скорость гидролиза (реакции с водой) сахарозы прямо пропорциональна молярной концентрации сахара и зависит от кислотности среды (концентрации кислоты в растворе).
-
Напишите формулу и уравнение реакции гидролиза сахарозы (массовая доля углерода в ней 42,11 %, а мольная – 26,67 %) [реакция 1]. Укажите тривиальные названия образующихся при этом продуктов. Попробуйте дать словесное определение скорости химической реакции, которая определяется следующим выражением:

Запишите другое уравнение (v(мгновенная) = ?), определяющее скорость реакции гидролиза сахарозы в момент времени, когда ее концентрация равна C(реагент). Как называется закон, описывающий это уравнение? В чем заключается различие между понятиями «средняя» и «мгновенная» скорость?
Решение задачи доступно только авторизованным пользователям — Войти
Решение
-
Все упомянутые уравнения в первом пункте, отличие средней от мгновенной скорости
Решение задачи доступно только авторизованным пользователям — Войти
Решение
-
Далее ТАРДИС перенесла Вас с Доктором в 1884 год к знаменитому ученому Якобу Хендрику Вант-Гоффу, который предложил конкретный коэффициент пропорциональности между скоростью реакции и молярными концентрациями реагирующих веществ – константу скорости реакции. Также Вант-Гофф предложил простое эмпирическое правило, учитывающее влияние температуры на константу скорости реакции (теперь оно известно как правило Вант-Гоффа): «При изменении температуры на 10 градусов константа скорости гомогенной реакции может изменяться в 2-4 раза (коэффициент γ) в зависимости от природы реагирующих веществ и выбранного интервала температур».
Для проведения дальнейших опытов необходимо приготовить 20 % по массе (ρ = 1,08 г/мл) раствор сахарозы и раствор соляной кислоты с концентрацией 4 моль/л (ρ = 1,07 г/мл).
В каком соотношении (массовом для сахарозы и объемном для соляной кислоты) необходимо смешать твердую сахарозу с водой и концентрированную соляную кислоту (ω(HCl) = 36,5 %, ρ = 1,18 г/мл) с водой для получения таких растворов?
Решение задачи доступно только авторизованным пользователям — Войти
Решение
-
При проведении реакции гидролиза сахарозы при 27 °С в течение 19 минут выход продуктов оказался равен 21,0 %, а при 38 °С (остальные параметры одинаковы) за 6 минут проведения реакции выход продуктов составил 16,5 %.
Используя формулы из п. 1, оцените значения констант скорости реакции (в мин-1 с точностью до тысячных) гидролиза сахарозы при двух указанных температурах. Для оценки примените приближение, позволяющее считать, что скорость реакции в момент определения выхода примерно равна средней скорости на участке от начала реакции до этого момента.
Решение задачи доступно только авторизованным пользователям — Войти
Решение
-
Оцените температурный коэффициент γ (с точностью до сотых) реакции гидролиза сахарозы.
Решение задачи доступно только авторизованным пользователям — Войти
Решение
-
Является ли функция k(T) линейной?
Решение задачи доступно только авторизованным пользователям — Войти
Решение
-
Как Вы думаете, от каких величин, помимо температуры, зависят рассчитанные Вами константы скорости
этой реакции?
Решение задачи доступно только авторизованным пользователям — Войти
Решение
-
Оцените молярные концентрации (с точностью до тысячных) соляной кислоты и сахарозы в указанные моменты времени для обоих опытов, если исходные растворы были смешаны в объёмном соотношении 1 : 1.
Решение задачи доступно только авторизованным пользователям — Войти
Решение
-
Помимо своего правила, Вант-Гофф предложил классификацию простых реакций на моно-, би- и тримолекулярные, в зависимости от числа молекул, при взаимодействии которых происходит превращение.
Предложите определение сложной реакции, если простая реакция представляет собой одностадийное превращение. Приведите по одному примеру простых реакций для каждого из предложенных Вант-Гоффом типов реакций. Как Вы думаете, почему не бывает тетра- и других полимолекулярных реакций? Является ли реакция гидролиза сахарозы простой?
Решение задачи доступно только авторизованным пользователям — Войти
Решение
-
Как Вы думаете, является ли реакция гидролиза сахарозы каталитической, или нет? Ответ обоснуйте. Попробуйте дать определение явлению катализа. Можно ли увеличить равновесный выход целевого продукта, добавив в систему катализатор?
Решение задачи доступно только авторизованным пользователям — Войти
Решение
-
В своем последнем на сегодня путешествии Вы посетили современную лабораторию в федеральном университете Висозы (Бразилия). В 2013 году большая работа в этой лаборатории была посвящена исследованию эффективности различных гетерополисоединений в качестве катализаторов окисления серосодержащих соединений пероксидом водорода. Справа представлена схема получения вещества X (синтезирован Ono по реакции [13], 1983 г.), являющегося одним из самых эффективных катализаторов. Исходные вещества являются основными компонентами природных минералов глинозема (бинарное A, массовая доля кислорода в котором составляет 47,06 %), молибденита (бинарное F) и фосфорита (J).
Если в реакцию [6] вступает 10 г вещества F, то в качестве одного из продуктов реакции образуется бесцветный газ объемом 2,8 л и плотностью 2,86 г/л (н. у.). В веществе H соотношение атомов азота и атомов кислорода равно 1 : 4, а металл находится в высшей степени окисления. При продолжительном выдерживании в вакууме над H2SO4 вещество I теряет 10 % своей массы. M и E реагируют в соотношении 1 : 1 с образованием вещества X, массовая доля фосфора в котором равна 1,676 %.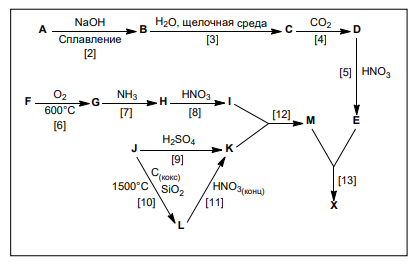
Решение задачи доступно только авторизованным пользователям — Войти
Решение

