«Рождающий А» (8 класс)
(для решения требуется авторизация)
Источник: Всесибирская олимпиада школьников по химии
Мировое потребление вещества X составляет около 75 млн тонн. Из них более 75 % производится каталитической водяной конверсией (реакция с парами воды) природного газа (его основным компонентом является метан CH4) при температурах порядка 1000 °С [реакция 1], а почти все остальное – паровой конверсией угля [2] при таких же температурах. После проведения реакций [1] и [2] полученную смесь газов X, Y (один из оксидов углерода) и водяных паров пропускают над катализатором при температуре 200-250 °С, проводя т.н. «реакцию водно-газового сдвига» [3]. В результате реакции газа Y и водяного пара получается газ Z (другой оксид углерода) и дополнительное количество газа X. Наиболее чистый X получают электролизом вещества A [4], в котором растворено некоторое количество щелочи для увеличения электропроводности A. Такой X представляет собой газ 99,7–99,8 % чистоты, а в виде примеси он содержит только воздух. Для очистки этот газ пропускают через башню с активной медью при нагревании, которая чернеет из-за образования ее оксида [5]. Затем газ пропускают через трубу с P2O5, который превращается в метафосфорную кислоту HPO3 [6]. Такой X можно применять для большинства лабораторных целей, так как присутствие незначительного количества нереакционноспособного газа B, являющегося основным компонентом воздуха, редко служит помехой.
-
Напишите формулы веществ X, A, B и уравнения реакций [1] – [6]. Внимание! Здесь и далее при написании реакций в ответ указывайте сумму минимальных целочисленных коэффициентов в записи их уравнений.
Решение задачи доступно только авторизованным пользователям — Войти
Решение
-
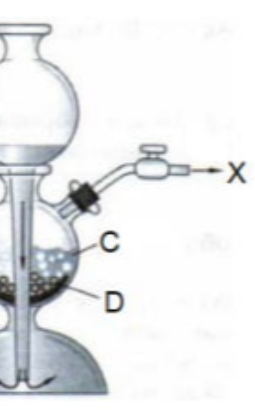
При помощи аппарата, представленного на рисунке, X обычно получают в лабораторных условиях посредством взаимодействия сложного вещества C с металлом D [7]. При этом из 13 г D можно получить до 4,88 л X (объем X измерен при 25 °C и 1 атм). Помимо этого, в результате реакции [7] образуется раствор вещества E с массовой долей металла в веществе 40,5 %.
Напишите формулы веществ C – E и уравнение реакции [7]. Назовите фамилию человека, который придумал аппарат, изображенный на рисунке. Рассчитайте массовую долю (в % с точностью до сотых) E в растворе, если для реакции с 13 г D использовать 700 мл 20 % раствора C с плотностью 1,14 г/мл.
Решение задачи доступно только авторизованным пользователям — Войти
Решение
-
Газ X в основном проявляет свойства восстановителя, но при этом почти всегда реагирует только при нагревании. Вам представлен список реагентов: Al2O3, CuO, I2, KOH, Fe2O3, CO. Не все из представленных веществ могут реагировать с X, реагирует лишь часть из них с образованием веществ 1 – черный порошок ω(O) = 27.59 % [9], 2 – красно-розовое простое вещество [10], 3 – бесцветный газ [11], 4 – бесцветный газ [12]. Известно, что 1 является компонентом распространенного минерала магнетита, а масса 1 л газа 3 в 8 раз меньше массы 1 л газа 4 (массы газов измерены при н.у.).
Отметим, что в реакциях [8-10] также образуется вещество A.
Из представленных выше веществ выберите те, которые могут реагировать с газом X
Решение задачи доступно только авторизованным пользователям — Войти
Решение
-
Напишите уравнения этих реакций [8] – [10] и формулы образующихся продуктов 1 – 4.
Решение задачи доступно только авторизованным пользователям — Войти
Решение
-
Предложите свой список из пяти сложных (в смысле не простых) веществ, которые могут реагировать с X при н.у. или при нагревании.
Решение задачи доступно только авторизованным пользователям — Войти
Решение
-
Предложите свой список из шести простых веществ, которые могут реагировать с X в каких-либо условиях (температура, давление, наличие катализатора). Учтите, что все элементы, образующие Ваши простые вещества, должны находиться в разных группах короткопериодного варианта Периодической системы (напр. Cu и Zn, но не Cu и K).
Решение задачи доступно только авторизованным пользователям — Войти
Решение